object(WP_Post)#14562 (24) {
["ID"]=>
int(5639)
["post_author"]=>
string(2) "23"
["post_date"]=>
string(19) "2022-04-30 12:37:33"
["post_date_gmt"]=>
string(19) "2022-04-30 11:37:33"
["post_content"]=>
string(7820) "Berlin (Deutschland), 30. April 2022 – Gefahr erkannt, Gefahr gebannt? Bei Clostridioides difficile-Infektionen (CDI) hat man sich damit in den vergangenen Jahren offenbar schwergetan. Die Morbiditäts- und Mortalitätsraten sind gestiegen.[1] In Europa und den USA haben die Fachgesellschaften daher die Leitlinien für eine effektive Therapie überarbeitet.[2],[3] Beim Tillotts-Symposium während des Kongresses der Deutschen Gesellschaft für Innere Medizin (DGIM) informierten Experten über den neuesten Stand bei Diagnostik und Therapie von C. diff.-Infektionen sowie die besonderen Implikationen bei Barriere-Störungen.
„Durchfall kann töten“1, weiß Magdalena Kritikos, Geschäftsführerin von Tillotts Pharma. „Auslöser kann ein Bakterium sein, das in der Umwelt und auch im Darm vorkommt: Clostridioides difficile. Der Erreger gilt als Krankenhauskeim, wird oft aber auch ambulant erworben. Besonders gefährdet sind Menschen, bei denen das Darm-Mikrobiom aus dem Gleichgewicht geraten ist – etwa durch eine Antibiotika-Behandlung, ein geschwächtes Immunsystem, eine chronisch-entzündliche Darmerkrankung oder anderes. Wir möchten mit unserem Symposium dazu beitragen, dass Ärztinnen und Ärzte besser über die möglichen Folgen einer Infektion informiert sind und die neuen Therapieempfehlungen kennen, um Patienten besser vor Rezidiven, Komplikationen und Schlimmerem zu bewahren.“
„C. difficile kann Toxine produzieren, welche die Intestinalzellen schädigen, eine Diarrhö auslösen und potenziell lebensbedrohliche Folgen haben können“, erläutert PD Dr. med. Stefan Hagel, M. Sc., vom Institut für Infektionsmedizin und Krankenhaushygiene am Universitätsklinikum Jena. „Ein zweistufiger Test gibt Sicherheit: Zunächst wird die Stuhlprobe mit einem hochsensiblen Nukleinsäure-Amplifikationstests (NAAT) oder Enzymimmunoassay (EIA) auf Glutamat-Dehydrogenase (GDH) geprüft. Ist der Nachweis positiv, wird mit einem EIA das spezifische Toxin festgestellt.[4] Bestätigt sich der Test, sollte C. difficile rasch therapiert werden. Herausfordernd ist dabei, dass bislang bei rund 20 Prozent der Patienten die CDI nach der Initialen Episode erneut aufflammte, über 30 Prozent hatten ein zweites oder drittes Rezidiv.“[5]
Fidaxomicin (Dificlir®): Therapie der 1. Wahl
„Für CDI-Patienten bedeutete dies ein erhöhtes Sterblichkeitsrisiko – nicht nur in der akuten Phase, sondern auch viele Monate über das initiale Abklingen der Infektion hinaus“[6], so Prof. Dr. Ahmed Madisch vom Centrum Gastroenterologie Bethanien in Frankfurt/Main. „Ein Wirkstoff zeigte jedoch einen besonders langfristigen Behandlungserfolg: Fidaxomicin. Das Antibiotikum wirkt selektiv und rasch gegen C. difficile, hat jedoch kaum negative Auswirkungen auf das restliche Darm-Mikrobiom, die Kolonisationsresistenz bleibt erhalten.[7] Es traten um fast die Hälfte weniger CDI-Rezidive auf als nach einer Therapie mit Vancomycin.[8] In Europa wie in den USA wird daher ab der initialen CDI-Episode und beim ersten Rezidiv nun Fidaxomicin als Standardtherapie empfohlen. Vancomycin ist 2. Wahl, Metronidazol sollte nur noch eingesetzt werden, wenn die ersten zwei Optionen nicht verfügbar sind.“2,3
„Ein fast fünffach erhöhtes Risiko für CDI haben Patienten mit chronisch-entzündlicher Darmerkrankung (CED) wie Morbus Crohn oder Colitis ulcerosa[9], besonders bei antibiotischer Therapie, Kolon-Manifestation und Biologika-Therapien.[10] Bei diesen Patienten ist die Darm-Barriere gestört“[11], gibt Prof. Dr. Dominik Bettenworth von der Praxis für Innere Medizin in Münster zu bedenken. Eine CDI ist hier häufiger Auslöser von CED-Schüben.[12] Es sollte daher frühzeitig abgeklärt werden, ob eine CDI vorliegt, um diese rechtzeitig und möglichst Mikrobiom-schonend zu therapieren.“12
[caption id="attachment_5417" align="alignnone" width="800"]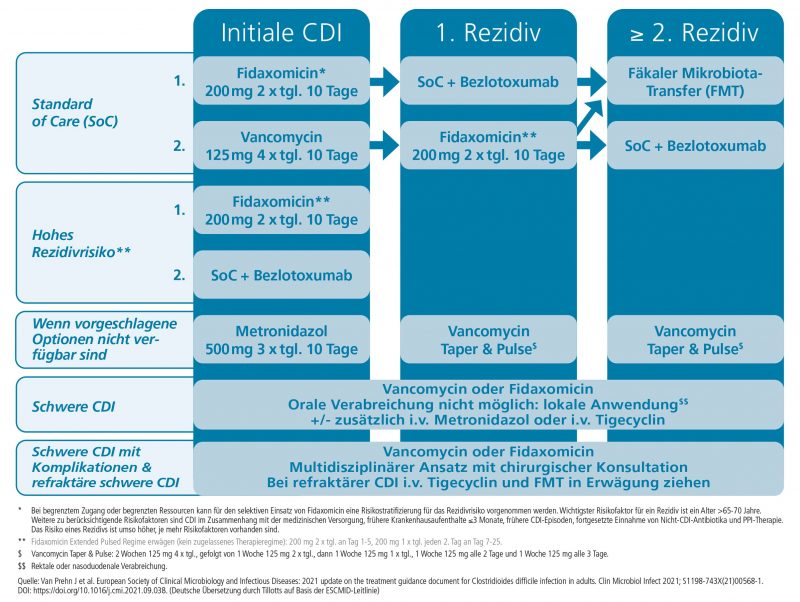 Abb. 1: Therapie-Algorithmus der neuen Europäischen Leitlinie zur Behandlung von Clostridioides-difficile-Infektionen (CDI). Quelle: European Society of Clinical Microbiology and Infectious Diseases (ESCMID) Treatment Guidance (Deutsche Übersetzung durch Tillotts auf Basis der ESCMID-Leitlinie1)[/caption]
[1] GBD 2016 Diarrhoeal Disease Collaborators. Lancet Infect Dis 2018;18:1211-1228.
[2] Van Prehn J et al. Clin Microbiol Infect 2021; 27 (Suppl 2):S1-S21.
[3] Johnson S et al. Clin Infect Dis 2021;73: e1029-e1044.
[4] Crobach MJ et al. Clin Microbiol Infect. 2016 Aug;22 Suppl 4:S63-81.
[5] Lübbert C et al. Infect Dis Ther 2016;5:545-554.
[6] Karas JA et al. Infect Dis Rep 2010;2:e8.
[7] Louie T et al. Clin Infect Dis 2012;55 (Suppl 2):S132-42.
[8] Louie TJ et al. N Engl J Med 2011; 364: 422-431.
[9] Singh H et al. Gastroenterology 2017;153:430-438.e2.
[10] Balram B et al. J Crohns Colitis. 2019 Jan 1;13(1):27-38.
[11] Neurath M Nat Rev Immunol. 2014 May;14(5):329-42.
[12] Sehgal K et al. Therap Adv Gastroenterol 2021; 14: 17562848211020285."
["post_title"]=>
string(64) "C. difficile-Infektionen: Therapie-Update beim Kongress der DGIM"
["post_excerpt"]=>
string(0) ""
["post_status"]=>
string(7) "publish"
["comment_status"]=>
string(6) "closed"
["ping_status"]=>
string(6) "closed"
["post_password"]=>
string(0) ""
["post_name"]=>
string(62) "c-difficile-infektionen-therapie-update-beim-kongress-der-dgim"
["to_ping"]=>
string(0) ""
["pinged"]=>
string(0) ""
["post_modified"]=>
string(19) "2024-04-18 14:44:46"
["post_modified_gmt"]=>
string(19) "2024-04-18 13:44:46"
["post_content_filtered"]=>
string(0) ""
["post_parent"]=>
int(0)
["guid"]=>
string(51) "https://www.tillotts.de/?post_type=news&p=5639"
["menu_order"]=>
int(0)
["post_type"]=>
string(4) "news"
["post_mime_type"]=>
string(0) ""
["comment_count"]=>
string(1) "0"
["filter"]=>
string(3) "raw"
}
Abb. 1: Therapie-Algorithmus der neuen Europäischen Leitlinie zur Behandlung von Clostridioides-difficile-Infektionen (CDI). Quelle: European Society of Clinical Microbiology and Infectious Diseases (ESCMID) Treatment Guidance (Deutsche Übersetzung durch Tillotts auf Basis der ESCMID-Leitlinie1)[/caption]
[1] GBD 2016 Diarrhoeal Disease Collaborators. Lancet Infect Dis 2018;18:1211-1228.
[2] Van Prehn J et al. Clin Microbiol Infect 2021; 27 (Suppl 2):S1-S21.
[3] Johnson S et al. Clin Infect Dis 2021;73: e1029-e1044.
[4] Crobach MJ et al. Clin Microbiol Infect. 2016 Aug;22 Suppl 4:S63-81.
[5] Lübbert C et al. Infect Dis Ther 2016;5:545-554.
[6] Karas JA et al. Infect Dis Rep 2010;2:e8.
[7] Louie T et al. Clin Infect Dis 2012;55 (Suppl 2):S132-42.
[8] Louie TJ et al. N Engl J Med 2011; 364: 422-431.
[9] Singh H et al. Gastroenterology 2017;153:430-438.e2.
[10] Balram B et al. J Crohns Colitis. 2019 Jan 1;13(1):27-38.
[11] Neurath M Nat Rev Immunol. 2014 May;14(5):329-42.
[12] Sehgal K et al. Therap Adv Gastroenterol 2021; 14: 17562848211020285."
["post_title"]=>
string(64) "C. difficile-Infektionen: Therapie-Update beim Kongress der DGIM"
["post_excerpt"]=>
string(0) ""
["post_status"]=>
string(7) "publish"
["comment_status"]=>
string(6) "closed"
["ping_status"]=>
string(6) "closed"
["post_password"]=>
string(0) ""
["post_name"]=>
string(62) "c-difficile-infektionen-therapie-update-beim-kongress-der-dgim"
["to_ping"]=>
string(0) ""
["pinged"]=>
string(0) ""
["post_modified"]=>
string(19) "2024-04-18 14:44:46"
["post_modified_gmt"]=>
string(19) "2024-04-18 13:44:46"
["post_content_filtered"]=>
string(0) ""
["post_parent"]=>
int(0)
["guid"]=>
string(51) "https://www.tillotts.de/?post_type=news&p=5639"
["menu_order"]=>
int(0)
["post_type"]=>
string(4) "news"
["post_mime_type"]=>
string(0) ""
["comment_count"]=>
string(1) "0"
["filter"]=>
string(3) "raw"
}